В основе патогенеза бронхиальной астмы лежит повышенная чувствительность и гиперреактивность бронхов на специфические и неспецифические раздражители. Это обусловливает спазм бронхов, их отек, гиперсекрецию слизи и дискринию. При всех нормах бронхиальной астмы наблюдается нарушение нейрогуморальных механизмов регуляции тонуса бронхов. Следует заметить, что тонус бронхов регулируется множеством факторов. Функциональное состояние бронхов регулируется парасимпатической и симпатической нервной системой, через ?-, ?1 и ?2-адренорецепторы и холинергические структуры, расположенные в большом количестве в стенке бронхов. Также в регуляции сокращения гладких мышц бронхов участвуют кальций и АТФ-зависимый кальциевый насос, клические нуклеотиды –цАМФ и цГМФ, продукты метаболизма арахидоновой кислоты – простагландины и лейкотриены, нейропептиды (тахикинины), которые обладают бронхоконстрикторными и бронходилатационными свойствами, цитокины, продуцируемые тучными клетками и лимфоцитами.
При анализе патофизиологических нарушений у больных бронхиальной астмой обнаружен дефект в биохимической структуре ?2-адренорецепторов, сводящийся к недостаточности аденилциклазы, снижение функции которой приводит к бронхоспазму, выявлены гиперчувствительность ?-адренорецепторов, и нарушения в холинергических структурах бронхов (повышение уровня ацетилхолина и снижение холинестеразы). Полагают, что нарушение равновесия между возбуждающими (?-адренергическая и холинергическая система) и ингибирующими (?-адренергическая система) механизмами тонуса бронхов является фактором их длительного спазма. У больных бронхиальной астмой также выявлена повышенная чувствительность ирритантных рецепторов, расположенных в слизистой оболочке верхних дыхательных путей, ответственных за бронхоспазм. У больных бронхиальной астмой, кроме того, повышена продукция ПГF2, обладающего бронхоконстрикторным действием. Нарушения в системе регуляции тонуса бронхов могут быть вызваны самыми различными факторами.
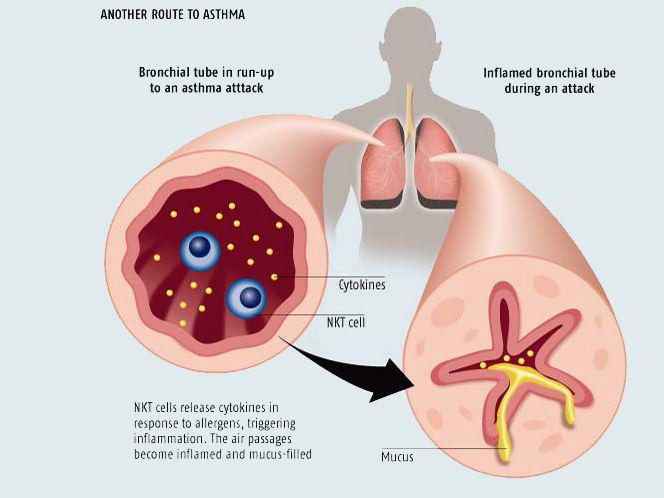
При аллергической бронхиальной астме развитие бронхоспазма и других проявлений заболевания вызывается аллергическими реакциями, развивающимися в тканях бронхиального дерева. В основе патогенеза неинфекционно-аллергической бронхиальной астмы лежат реакции гиперчувствительности I типа. В результате аллергизации организма у больных формируются IgЕ-специфические антитела, которые фиксируются на тучных клетках и базофилах крови. При повторном попадании аллергена в организм происходит его взаимодействие с фиксированными IgЕ, что приводит к выбросу из тучных клеток медиаторов воспаления (гистамина, ацетилхолина, серотонина, протеаз, фактора хемотаксиса эозинофилов, нейтрофилов) и стимуляция метаболизма мембранных фосфолипидов. Первичные медиаторы воспаления и продукты метаболизма арахидоновой кислоты – простагландины (РGD2) и лейкотриены (LTC4) вызывают повышение проницаемости сосудистого русла, отек слизистой оболочки дыхательных путей, спазм гладкой мускулатуры бронхов, инфильтрацию ткани эозинофилами, нейтрофилами, усиливают секрецию бронхиальных желез. Перечисленные процессы развиваются в течение первых 5-20 минут после контакта организма с аллергеном и могут самостоятельно угаснуть через 1-2 часа.
У части больных через 4-6 часов наблюдается повторный бронхоспазм, который может продолжаться сутки и более. Он опосредуется вторичными медиаторами тучных клеток: фактором активации тромбоцитов, лейкотриенами (LTC4), а также хемотаксинами эозинофилов и нейтрофилов. Медиаторы поздней реакции индуцируют хемотаксис клеток в зону воспаления, вызывают активацию клеток воспаления в слизистой оболочке бронхов и стимулируют синтез лейкотриенов. Кроме перечисленных медиаторов, в развитии воспалительной реакции в бронхах участвуют активные формы кислорода, кинины, тромбоксаны, протеазы, цитокины (ИЛ-1, ИЛ-6, ФНО?).
В основе патогенеза инфекционно-аллергической бронхиальной астмы лежат аллергические реакции немедленного и замедленного типов. В результате сенсибилизации организма микробными антигенами появляются специфические антитела (IgЕ и IgG) и сенсибилизированные лимфоциты. У больных этой формы бронхиальной астмы из содержимого бронхов высеваются около 14 видов условно-патогенных и сапрофитных микроорганизмов. Чаще определяются Neisseria perflava, staphylococcus aureus, Klebsiella pneumoniae, которые, как установлено, имеют общие антигенные детерминанты с тканями легких человека. Бронхоспазм при бронхиальной астме индуцируется медиаторами, высвобождаемыми из тучных клеток (гистамин, серотонин, ацетилхолин, лейкотриены и др.) в результате взаимодействия на их поверхности антигена с фиксированными антителами и медиаторами, выделяемыми антигенактивированными сенсибилизированными лимфоцитами (цитокины, HRF-histamine releasing factor). HRF, продуцируемый лимфоцитами, стимулирует высвобождение из тучных клеток гистамина и других биологически активных веществ. Кроме того, бактериальные антигены способны самостоятельно индуцировать сокращение гладких мышц бронхов в результате прямого воздействия на них.
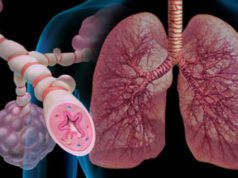
При приступах бронхиальной астмы сужение бронхов развивается в результате спазма гладких мышц, образования слизистых пробок, отека и воспаления слизистой оболочки. Обструкция усиливается во время выдоха, поскольку при этом происходит динамическое сужение дыхательных путей. Из-за сужения бронхов часть воздуха задерживается в альвеолах, что приводит к перерастяжению легких и удлинению выдоха. Избыточное сопротивление дыхательных путей приводит к напряжению в легких, в акт дыхания включаются дополнительные мышцы, появляется одышка. Образующаяся при бронхиальной астме густая, вязкая слизь содержит слущенный эпителий бронхов, эозинофилы, кристаллы Шарко-Лейдена. Слизь способна частично и полностью закупоривать бронхи. Чем длиннее и тяжелее приступ, тем более вязкой становится слизь из-за дегидратации. При бронхиальной астме активно протекает процесс морфологической перестройки стенки бронхов. Происходит уменьшение количества клеток мерцательного эпителия, увеличивается число клеток, секретирующих слизь, возникает эозинофильная, лимфоцитарная и макрофагальная инфильтрации ткани бронхов, отек и утолщение базальной мембраны, гипертрофия мышечной оболочки бронхов.
При бронхиальной астме в патологический процесс вовлекаются крупные, средние и мелкие бронхи. Шумное свистящее дыхание наблюдается при обструкции крупных бронхов, а приступы одышки и кашля развиваются при обструкции мелких бронхов.
Обструкция бронхов во время приступа бронхиальной астмы приводит к увеличению остаточного объема (ОО), уменьшению жизненной емкости легких (ЖЕЛ) и повышению общей емкости легких (ОЕЛ). Выраженность этих изменений зависит от тяжести приступа. Остаточный объем легких во время приступа может превышать значение общей емкости легких в межприступный период. Обструкция бронхов во время приступа неравномерна, поэтому одни участки легких могут вентилироваться лучше, а другие – хуже. Перфузия плохо вентилируемых участков резко снижается, нарушается равновесие между вентиляцией и перфузией, что приводит к снижению парциального давления O2 в артериях (раO2). В легких случаях это может быть единственным отклонением от нормы в газовом составе крови. Уровень парциального давления CO2 в артериях (раCO2) зависит от вентиляции альвеол. При легких и среднетяжелых приступах бронхиальной астмы возникает гипервентиляция, которая приводит к уменьшению раCO2 и дыхательному алкалозу. При тяжелых и длительных приступах, напротив, развивается гиповентиляция, повышается раCO2 и возникает дыхательный ацидоз. Перерастяжение легких и снижение парциального давления O2 в альвеолах (раO2) вызывают сужение капилляров альвеол и повышение давления в легочной артерии. Чем тяжелее приступ бронхиальной астмы, тем более выражена легочная гипертензия.