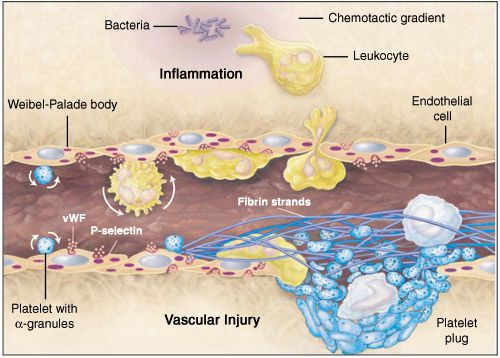
Активным участником воспалительной реакции являются эндотелиальные клетки сосудов. Они играют важную роль в регуляции сосудистого тонуса и тканевой перфузии, обусловленной действием сосудорасширяющих (например, ПГI2, аденозина, NO) и сосудосуживающих (например, эндотелина) веществ. Нарушение функции эндотелиальных клеток или их деструкция приводят к агрегации тромбоцитов, лейкоцитов и формированию внутрисосудистых тромбов. Эндотелиальные клетки являются продуцентами ряда биологически активных веществ и цитокинов (ИЛ-1, ИЛ-8, ИЛ-6). Под влиянием микробных факторов и медиаторов воспаления функции эндотелиальных клеток нарушаются. В нормальных условиях эндотелий сосудов регулирует и контролирует движение макромолекул и лейкоцитов в ткани, где лейкоциты осуществляют контроль за антигенным гомеостазом организма. Этот процесс обеспечивается гликопротеиновыми молекулами, получившими название молекул клеточной адгезии (САМ), которые экспрессированы на поверхности эндотелиальных клеток. На эндотелиальных клетках экспрессированы Р- и Е-селектины, муциноподобные адрессины – CD34, GlyCAM-1, MadCAM-1, молекулы суперсемейства иммуноглобулинов – ICAM-1, ICAM-2, VCAM-1.
При развитии воспаления происходит повышенная экспресия адгезивных молекул на эндотелиоцитах, они обеспечивают аккумуляцию лейкоцитов в микроциркуляторном русле зоны воспаления и их экстравазацию в ткань. Воздействие на эндотелиальные клетки микробных токсинов, провоспалительных цитокинов, тромбина, гистамина, оксидантов, компонентов комплемента С5b-С9 приводит к повышенной экспрессии Р-селектинов. Экспрессия этих гликопротеиновых молекул на клетках является самым ранним событием воспалительного процесса. Это, вероятно, связано с тем, что синтеза этих макромолекул de novo не требуется, так как они всегда имеются в клетке в готовом виде. Экспрессия Е-селектинов на эндотелиоцитах несколько запаздывает по сравнению с Р-селектинами. Их экспрессия требует синтеза этих молекул de novo. Под влиянием различных факторов воспаления на эндотелиоцитах повышается экспрессия VСАМ-1 (например, под воздействием Н2О2), ICAM-1 (например, под воздействием лизофосфатидилхолина). На активированных лейкоцитах также, в свою очередь, повышается экспрессия молекул, отвечающих за межклеточные взаимодействия (LFA-1, MAC-1 (CD116/CD118), VLA-4, LFA, L-селектина). Повышенная экспресия молекул межклеточных взаимодействий на эндотелиальных клетках сосудов и лейкоцитах обеспечивает эффективное и более плотное «сцепление» клеток, что, в свою очередь, способствует концентрированию нейтрофилов, базофилов, эозинофилов, моноцитов, лимфоцитов в области «воспаленных» сосудов и концентрации патогена. Отсюда клетки под влиянием хематаксических факторов мигрируют в воспаленную ткань. Процесс эксвазации лейкоцитов является активным событием. Первичное взаимодействие активированных лейкоцитов (нейтрофилов, лимфоцитов) с эндотелиальными клетками сосудов осуществляется благодаря взаимодействию L-селектинов лейкоцитов и Р- и Е-селектинов эндотелиоцитов с соответствующими контрлигандами. L-селектины лейкоцитов взаимодействуют с GlyCAM-1, CD34, MadCAM-1- адрессиновыми молекулами эндотелия, а Р- и Е-селектины-с сивалилом Левиса лейкоцитов. Это взаимодействие обеспечивает «роллинг» (прокатывание) лейкоцитов по стенке сосуда. Взаимодействие интегринов лейкоцитов LFA-1, VLA-4, VLA-5, Mac-1 (CD11b/CD18) с молекулами ICAM-1,2,3, VCAM-1, MadCAM-1 эндотелиоцитов обеспечивает плотный контакт между клетками и закрепление лейкоцитов на стенке сосуда. Воздействие дополнительных активационных сигналов на лейкоциты, которыми могут являться и хемокины, инициирует миграции клеток сквозь сосудистую стенку в ткань. Эндотелиальные клетки, стимулированные бактериальными эндотоксинами и провоспалительными цитокинами также секретируют низкомолекулярные пептиды с хемотаксическими свойствами.
Адгезия и эксвазация лейкоцитов находятся под контролем множества факторов, в том числе и цитокинов. ИЛ-1, ФНО-α, ИЛ-4, ИЛ-8, ИНФ-γ стимулируют эти процессы, а ТФРβ и ГМ-КСФ – подавляют.