Эксперименты на животных показали, что организм на опухолевые антигены способен развивать как гуморальные, так и клеточные иммунные реакции. При этом следует учитывать, что развитие иммунного ответа происходит только в случае, если опухолевые клетки содержат антигены, чужеродные организму хозяина (например, опухоле-специфические антигены). Достоверно установлено развитие иммунных реакций на вирус-индуцированные опухоли и опухоли, вызванные химическими веществами и облучением. Опухоли, экспрессирующие раковоэмбриональные антигены или опухолеассоциированные белки, которые представлены рецепторными молекулами или факторами роста, как правило, не индуцируют иммунные реакции.
Основную роль в противоопухолевом иммунитете играют клеточные реакции.
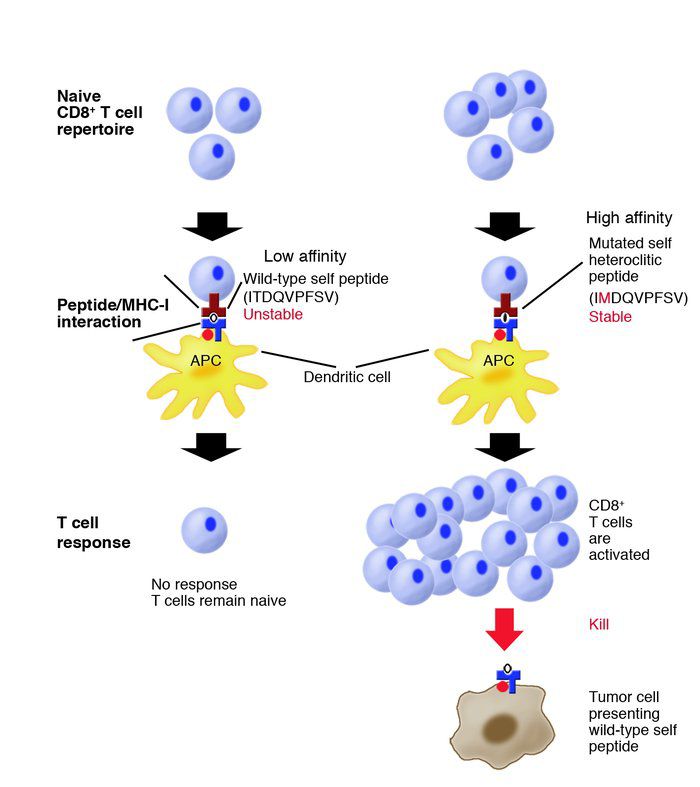
В эксперименте на животных показано, что опухоли способны индуцировать образование специфических эффекторных Т-киллеров, которые, распознавая опухолевые антигены на клетках, представленные в комплексе с молекулами HLA- 1 класса, вызывают их цитолиз. Лизис опухолевых клеток происходит за счет продукции лимфоцитами перфоринов, фрагментинов и индукции апоптоза через Fas-лиганды. Способность Т-цитотоксических лимфоцитов вызывать разрушение опухолевых клеток также показана в экспериментах ин витро. Если от животных с вирусиндуцированной опухолью получить клетки лимфатических узлов и добавить их к культуре опухолевых клеток той же линии, то через несколько часов наблюдается лизис всех опухолевых клеток. Замечено, что по мере роста ряда опухолей противоопухолевая активность Т-киллеров снижается. Установлено, что это связано с тем, что в процессе развития опухоли опухолевые клетки существенно снижают либо полностью прекращают экспрессию молекул HLA 1 класса, что значительно ограничивает литический потенциал Т-киллеров.
В отличие от Т-цитотоксических лимфоцитов, распознавание НК-клетками опухолевых антигенов не рестриктировано антигенами HLA. Их цитотоксическая активность не снижается с уменьшением экспрессии этих молекул. Они способны оказывать как прямое цитотоксическое действие на опухолевые клетки, так и через развитие реакции антитело-зависимой клеточной цитотоксичности (АЗКЦ), в которой специфические противоопухолевые антитела своим активным центром соединяются с опухолевой клеткой, а через Fc-фрагмент присоединяют НК-клетку. Механизм цитолиза клеток НК-лимфоцитами аналогичен тому, который используют Т-киллеры.
Макрофаги свое цитотоксическое действие на опухоли оказывают через развитие реакции АЗКЦ, либо в процессе прямого контакта с опухолевой клеткой. При этом гибель клеток происходит в результате воздействия на них активных форм кислорода, оксида азота, литических энзимов, фактора некроза опухоли альфа (ФНО?), который обладает высокой противоопухолевой активностью. Известно, что введение животным с опухолью ФНО? приводит к развитию множественных геморрагий в опухоли и ее некрозу. Действие ФНО? усиливается интерфероном-альфа. В активации макрофагов и концентрировании их вокруг опухоли большую роль играют ИНФ-? и Т-лимфоциты хелперы. Интерферон-гамма также активирует НК-клетки. Важную роль в стимуляции противоопухолевой активности Т-цитотоксических лимфоцитов, макрофагов и НК-клеток играет ИЛ-12.
Гуморальные иммунные реакции при опухолевом росте могут как способствовать регрессии опухоли, так и стимулировать ее развитие. Установлено, что взаимодействие антител с некоторыми опухолевыми клетками приводит к активации комплемента и лизису опухолевых клеток. Антитела также выступают индукторами реакции антитело-зависимой клеточной цитотоксичности. Проведенные опыты на инбредных мышах показали, что антительный иммунный ответ может быть более эффективным в защите от химически индуцированных опухолей, чем макрофагальная противоопухолевая активность.
Вместе с тем, было замечено, что усиление гуморальной иммунной реакции часто способствует росту опухоли. Это отмечалось как при попытках защитить животных от опухолевого роста с помощью активной иммунизации опухолевыми антигенами, так и при пассивной иммунизации животных путем введения специфических антиопухолевых антител. Также обнаружено, что сыворотка, полученная от животных с прогрессирующим опухолевым ростом, блокирует литическое действие лимфоцитов в реакции клеточно-опосредованной цитотоксичности. Исследователи наблюдаемый эффект усиления опухолевого роста связывают с маскировкой антителами специфических детерминант опухолевых клеток, что блокирует развитие клеточных иммунных реакций. Установлено, что подобный эффект оказывают также иммунные комплексы (ИК), формируемые антителами с растворимыми опухолевыми антигенами.
Суммируя вышеизложенное, можно заключить, что рост опухоли может происходить:
1) либо в результате прорыва иммунной защиты организма, как это справедливо в отношении вирус-индуцированных опухолей;
2) либо в результате «иммунной невидимости» опухолевых клеток, как это отмечается при большинстве спонтанных опухолей, которые не несут опухолеспецифических антигенов.